

基因组每时每刻都遭受着来自内外源各种因素引起的DNA损伤。机体通过不同的DNA修复机制来纠正和修复损伤,维持基因组稳定性。碱基切除修复(BER)是机体维持基因组稳定的一线修复途径,可以有效地修复多种DNA损伤类型,包括各种DNA碱基损伤和单链断裂。作为细胞抵抗损伤的主要防御手段,BER过程的失调或功能障碍与多种疾病密切相关,包括神经退行性疾病、衰老、肿瘤和化疗抵抗等。尽管BER的各个步骤已经基本清楚,但BER组分的动态调控在很大程度上仍是未知的。
2022年7月19日,美高梅登录正网基础医学院罗建沅/王海英团队在Cell Reports杂志上在线发表了题为Acetylation of p62 regulates base excision repair through interaction with APE1 的研究论文,报道了hMOF和SIRT7动态调控p62 K264位点的乙酰化,乙酰化的p62通过促进BER通路中的关键酶APE1染色质募集和酶活性,从而促进碱基切除修复。

研究人员发现敲除p62的细胞对氧化剂和烷化剂更为敏感,表明p62是BER有效修复所必需的。当烷化剂甲磺酸甲酯诱导DNA损伤时,p62乙酰化水平升高。通过质谱分析鉴定及体内和体外的乙酰化、去乙酰化实验发现hMOF为p62 K264位点的乙酰基转移酶,SIRT7为其去乙酰化酶。接着通过染色质组分分离,APE1酶活性测定等实验,研究人员发现p62 K264乙酰化在BER中发挥重要的调控作用。乙酰化的p62与APE1相互作用并促进APE1染色质募集和提高APE1的脱碱基核酸内切酶活性,从而提高BER效率,促进细胞存活。
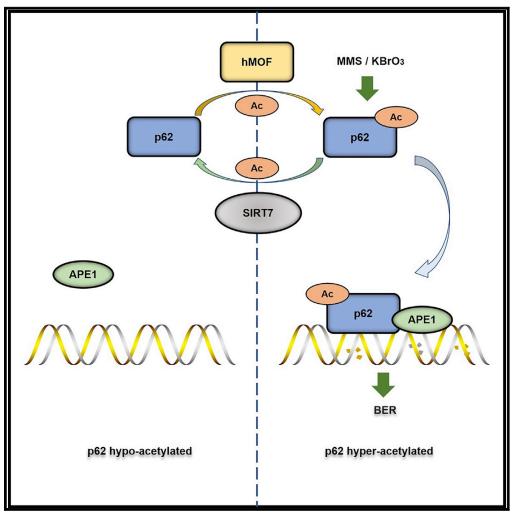
p62作为细胞自噬的重要受体蛋白,之前的研究发现其参与调控DNA双链损伤修复,本研究发现了hMOF和SIRT7共同调控p62 K264位点的乙酰化,从而调控碱基切除修复的新机制。这项研究不仅为p62在DNA损伤修复中的作用提供了新的证据,也为基于DNA损伤修复机制研发的药物提供新的研究方向,给有效治疗疾病提供了新线索。
美高梅登录正网博士后李美婷,基础医学院硕士熊健楠为该文章的共同第一作者,美高梅登录正网王海英副教授和罗建沅教授为该工作的共同通讯作者。该工作得到了国家自然科学基金面上项目、国家重点基础研究计划和美高梅登录正网医学科技创新平台发展基金—医学交叉种子基金资助项目的支持。
原文链接:
https://doi.org/10.1016/j.celrep.2022.111116
(美高梅登录正网基础医学院)